Исследуемый материал
Смотрите в описании
Метод определения
Гистологическое исследование биоптата согласно гистологической классификации Всемирной организации здравоохранения (ВОЗ) с окрашиванием гематоксилином-эозином. ИГХ-исследование с применением спектра антител (пероксидазный и авидин-биотиновый методы).
Комплексное исследование биоптатов метастатических образований различных локализаций, включающее морфологическое описание и оценку экспрессии спектра тканевых маркеров, для определения гистогенеза первичного опухолевого очага.
По статистике, в 3-15% случаев злокачественные опухоли манифестируют метастазами. Метастазы без выявленного первичного очага характеризуются случайной, нетипичной локализацией и быстрым прогрессированием процесса. Средняя продолжительность жизни пациентов с тремя и более метастатическими очагами поражения составляет три месяца. При этом локализация первичного очага у 60-70% пациентов выявляется только на аутопсии. Своевременная ИГХ-диагностика определяет тактику лечения до выявления первичного очага.
Патоморфологическая диагностика метастазов невыявленных опухолей предусматривает определение их морфологического типа, уточнение вероятного источника метастазирования, оценку злокачественного потенциала. Первая задача решается при рутинном гистологическом исследовании биопсийного материала (окрашивание гематоксилином-эозином), вторая – применением специальных методов исследования: гистохимического, иммуногистохимического (ИГХ) или молекулярно-генетического метода FISH (Fluorescence In Situ Hybridization).
При рутинной морфологической диагностике метастатические опухоли, согласно рекомендациям Европейского общества медицинской онкологии ESMO (European Society for Medical Oncology) (2004), разделяются на пять крупных категорий: аденокарцинома, плоскоклеточный рак, нейроэндокринный рак, недифференцированный рак, недифференцированная опухоль. Эти морфологические категории, наряду с данными о распространенности процесса, во многих случаях позволяют определить адекватный план обследования (и лечения). Так, например, при выявлении метастаза плоскоклеточного рака в шейных лимфатических узлах необходимо эндоскопическое обследования органов верхних дыхательных и пищеварительных путей. ИГХ-исследование, в зависимости от морфологического типа новообразования, позволяет уточнить гистогенез опухоли и/или определить вероятную локализацию первичного очага.
Для ИГХ-исследования первичных опухолей и их метастазов используется широкий спектр тканеспецифичных маркеров: -цитоспецифичные (кластеры дифференцировки лейкоцитов (CD – Clusters of Differentiation), гладкомышечный актин, миоглобин, тиреоглобулин); -маркеры пролиферации (Ki67, PCNA – Proliferating Cell Nuclear Antigen); -опухолевые маркеры – онкофетальные антигены (фетопротеин, карциноэмбриональный антиген); -гормоны (эстроген, прогестерон); -ферменты, белковые продукты клеточных онкогенов и др.
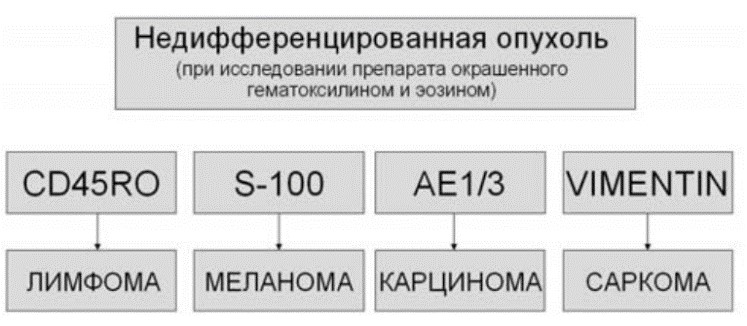
Единых алгоритмов при ИГХ-исследовании метастазов опухолей без уточненного первичного очага не разработано. Корректное определение направления дифференцировки опухолевых клеток и ряда биологических параметров опухоли само по себе является показанием для назначения определенных схем терапии. Например, обнаружение метастазов аденокарциномы в лимфоузлах подмышечной области может являться показанием к проведению терапии, аналогичной терапии рака молочной железы соответствующей стадии. Обнаружение экспрессии рецепторов эстрогенов и прогестерона в такой аденокарциноме может стать показанием к назначению антигормональной терапии вне зависимости от наличия определяемого опухолевого узла в молочной железе. Пример алгоритма, рекомендуемого для использования в дифференциальной диагностике.
Материал для исследования: биоптат опухоли, фиксированный в забуференном 10% растворе формалина.
Литература
- Blaszyk H., Hartmann A., Bjornsson J. Cancer of unknown primary: clinicopathologic correlations. APMIS. 2003;111(12):1089-1094.
- Dabbs D.J. Diagnostic Immunohistochemistry: Theranostic and Genomic Applications. Elsevier, 4-th Edition. 2013:960.
- Di Patre P.L., Carter D. Sternberg"s Diagnostic Surgical Pathology Review. Wolters Kluver, 2-nd Edition. 2015:488.
- Dietal M., Wittekind С., Bussolati G., von Winterfeld М. Pre-Analytics of Pathological Specimens in Oncology. Sрringer. 2015:133.
- Dodd L.G, Bui M.М. Atlas of Soft Tissue and Bone Pathology. DemosMEDICAL. 2014:720.
- Edge S.B, Byrd D.R., Compton C.C., Fritz A.G., Greene F.L., Trotti A. AJCC Cancer Staging Manual. Sрringer, 7-th Edition. 2011:646.
- Elder D.E. Lever"s Histopathology of the Skin. Wolters Kluver, 11-th Edition. 2014:1544.
- Epstein J., Netto G. Biopsy Interpretation of the Prostate. Lippincott Williams and Wilkins, 5-th Edition. 2014:450.
- Erickson L. Atlas of Endocrine Pathology. Sрringer, 1-st Edition. 2014:178.
- ESMO Minimum Clinical Recommendations for diagnosis, treatment and follow-up of cancers of unknown primary site. Annals of Oncology. 2005;16(S.1):175-176.
- Fletcher C.D.M., Bridge J.A., Hogendoorn P., Mertens F. WHO Classification of Tumours of Soft Tissue and Bone. WHO Press, 4-th Edition. 2013;5:427.
- Kurman R.J., Carcangiu M.L., Herrington C.S., Young R.H. WHO Classification of Tumours of the Female Reproductive Organs. WHO Press, 4-th Edition. 2014;4:316.
- Louis D.N., Ohgaki H., Wiestler O.D., Cavenee W.K. WHO Classification of Tumours of the Central Nervous System. WHO Press, 4-th Edition. 2007;1:312.
- Malpica A., Euscher Е.D. Biopsy Interpretation of the Uterine Cervix and Corpus. Wolters Kluver, 2-nd Edition. 2015:368.
- Nishizuka S., Chen S.T., Gwadry F. et al. Diagnostic markers that distinguish colon and ovarian adenocarcinomas: identification by genomic, proteomic, and tissue array profiling. Cancer Research. 2003;63:5243-5250.
- Nordi Q.C. http://www.nordiqc.org.